▼ Exp4. 몰질량 측정 레포트 보러가기 ▼
일반화학실험#4 몰질량 측정(Molar Mass Determination) 만점보고서(레포트), 내용총정리
레포트 만점 받았어요~!! 뿌이뿌이뿌이 소리질럿 ??: 내가 왜.... Exp4. Molar mass determination (몰질량 측정) 영어내용은 파파고에 복붙하시면 보기 쉬울 거에요 *대학교에서는 다 영어로 하기 때문에
young-brightening.tistory.com
Exp5. Analysis of Carbonate Salt (탄산염 분석)
🧪 일반화학실험 4번째 포스팅
✔ 대학교 수업자료는 영어로 제공되기
때문에 영어내용이 포함되어 있습니다.
영어내용은 한국어로도 적어둘게요
(순서: 영어 - 한국어)
한국어로 번역이 안 되어 있는 내용은
파파고에 복사붙여넣기 하시면
내용을 쉽게 읽으실 수 있어요 ˘◡˘

✔ 많은 고등학생/대학생 분들께
실험 내용을 알려드리기 위해
작성한 포스팅입니다.
표절을 하게 되면 유사도검사를
통해 불이익을 받을 수 있습니다.
참고 교재


General Chemistry Laboratory 7th Edition
(표준 일반화학실험 제7개정판)
저자 대한화학회
출판 천문각
1. 실험목적
탄산염이 염산과 반응할 때 발생하는 이산화탄소의 부피를 측정하여 탄산염의 종류를 알아낸다.

모두 탐정이 되어봅시다. (비장)
2. 실험원리 / 이론적배경
교과서 내용
(제가 필기한 내용이나 형광펜 친 부분들 위주로 보면 공부하기 더 좋으실 거에요!)



필기한 파일이 일반 백지보다 눈에 더 잘들어오는거 알져 >_0
3. 준비물 :실험기구 및 시약
<실험기구>
- 50mL 뷰렛
- 100mL 삼각 플라스크
- 고무 마개와 유리관
- 고무관
- 스탠드
<시약>
- 알칼리 금속의 탄산염
- Li2co3 (lithium carbonate)
- Na2CO3 (sodium carbonate)
- K2CO3 (potassium carbonate)
- 6M HCl(aq) (hydrochloric acd)
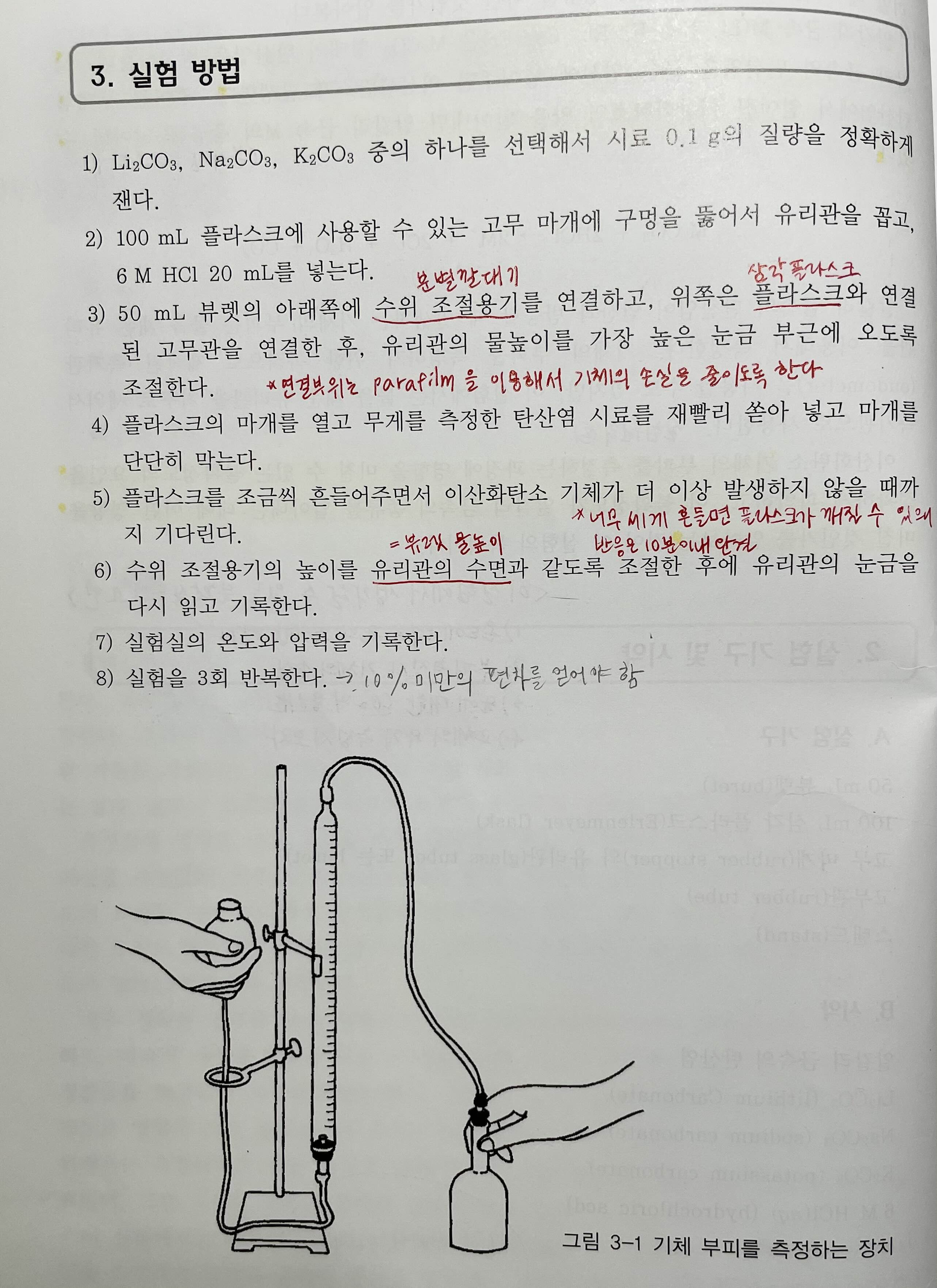
4. 실험방법
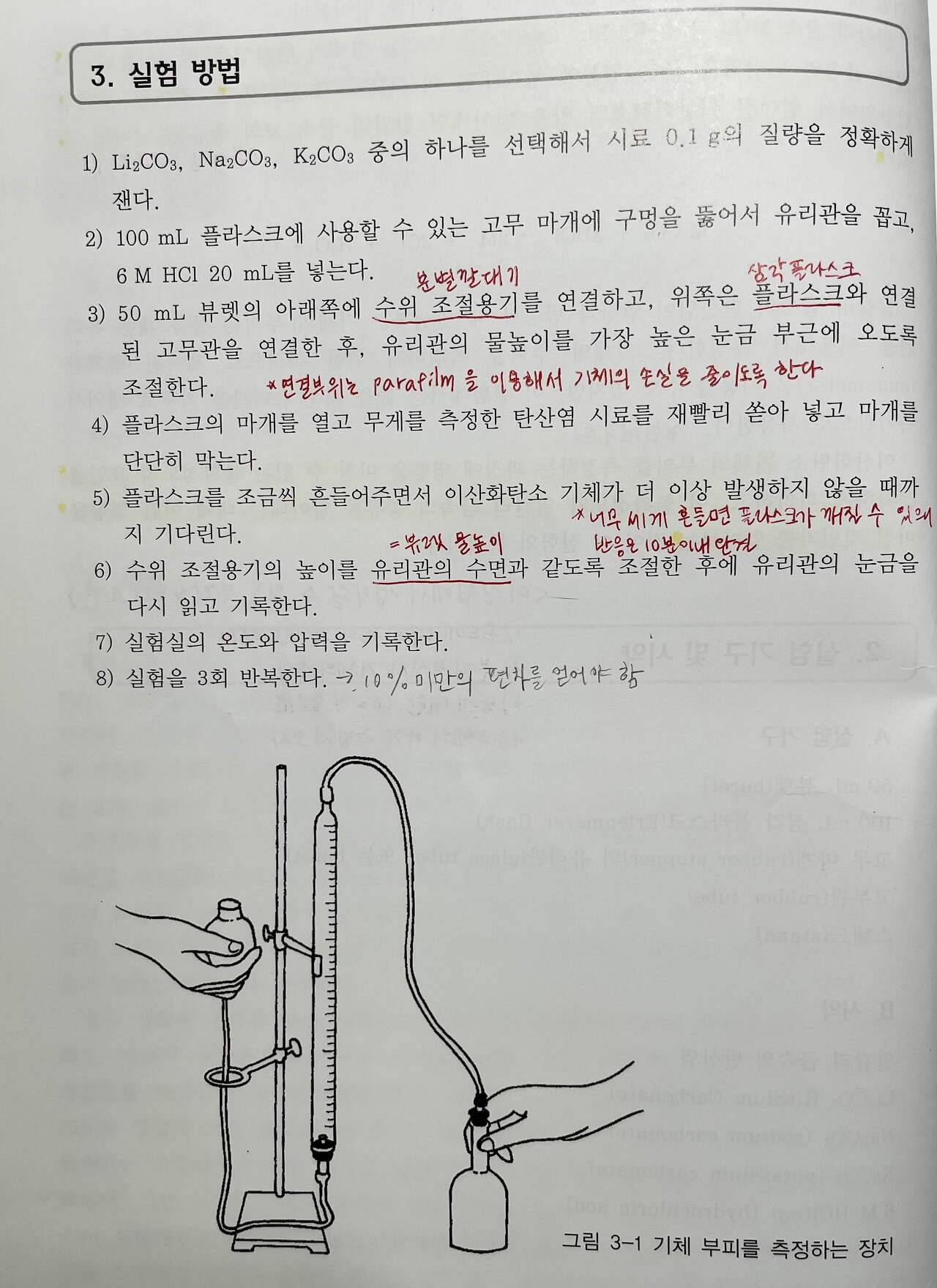
교재 44page 참고
5. 실험결과

1. In the experiment, 6 M HCl was used. What mL of HCl (37.0 %) solution is required to make 20 mL of 6 M HCl? (Density of 37.0 % HCl: 1.20 g/mL, molecular weight of HCl: 36.46 g/mol) (Show your calculation) (5 points)
Answer of 1
37%는 100g에서 37g만큼 존재하는 것과 같으니
37g/100g solution*1.20g.mL*1mol/36.46g/1000Ml/1L=12.18M
따라서 6M HCL 20Ml에 들어있는 HCL몰수는 0.12mol
2. Fill in the blanks. (Show your calculation) (10 points)
| Weight of sample | 0.103 g |
| Volume of CO2 gas | 21.5 mL |
| Temperature | 10 ℃ |
| Pressure | 1 atm |
| Moles of CO2 gas | 9.25*(10^(-4))mol |
| Molecular weight of unknown sample | 111.35g/mol |
* Universal gas constant is 0.08206 L∙atm/mol∙K and 0 ℃ = 273.15 K.
Answer of 2 (위 빈칸포함)
-PV=NRT에서 N=PV/RT
N=1atm*0.0215L/283.15K*(008206L*atm/mol*K)
=9.26*(10^(-4)) mol
-0.103g/9.25*(10^(-4))mol=111.35g/mol
3. The water vapor pressure was not considered to obtain the above results. Calibrate the moles of CO2 gas and molecular weight of the sample by considering the water vapor pressure with temperature. (1 atm=760 mmHg) (Show your calculation) (8 points)

Answer of 3 (빈칸)
* Water vapor pressure = ( 9.209 ) mmHg
* Corrected pressure = ( 750.791) mmHg (1 points)
= ( 0.987 ) atm (1 points)
* Moles of CO2 gas = ( 9.13*(10^(-4)) ) mol (3 points)
* Molecular weight of the sample = ( 112.77 ) g/mol (3 points)
4. According to the above results, which of the following is the unknown sample? (3 points)
① Li2CO3=73.891 g/mol
② Na2CO3=105.9884 g/mol (anhydrous)
③ K2CO3=138.205 g/mol
Answer of 4
2번 Na2CO3
5. Describe why the molar mass obtained from the experiment differs from the actual value. (4 points)
Answer of 5
온도에 따른 물의 증기압 변화, 부피 측정시 기체의 손실, 물에 대한 CO2의 용해도, 고체의 무게 측정 시 오차 때문에 차이가 있을 수 있다.
6. 주의 및 참고사항
<이 실험에서 생각할 수 있는 불확실도의 요인>
1) 온도에 따른 물의 증기압 변화
2) 부피 측정 시 기체의 손실
3) 물에 대한 CO2 용해도
4) 고체의 무게 측정 시 오차
7. 레포트 자료 구매 안내
해피캠퍼스 플랫폼을 통해 유료로 화학실험 레포트들을 구매하실 수 있습니다
(아래 링크를 통해 둘러보실 수 있어요)
완충용액 (Buffer Solution)
일반화학실험2 완충용액 레포트 레포트
A. Objectives 완충 용액의 원리를 탄산같은 이양성자산의 적정 곡선을 통하여 배운다. 실험에서는 염산 수용액으로 탄산염 수용액을 적정하면서 탄산이온이 모두 소모되는 제1 종말점과 중탄산이
www.happycampus.com
평형상수와 용해도곱 결정
일반화학실험2 평형상수와 용해도곱 결정 레포트 레포트
A. Objectives 색깔을 비교하는 방법(비색법)을 이용해 착이온의 농도를 알아내어 착이온 생성 반응의 평형상수를 결정하고, 포화 용액에 공통이온 효과를 이용해서 용해도곱을
www.happycampus.com
촉매반응
일반화학실험2 촉매반응 레포트 레포트
A. Objectives 과산화수소의 분해 반응을 빠르게 하는 다양한 촉매와 반응을 느리게 하는 억제제의 작용과 그 원리를 알아본다. 화학 반응의 속도를 변화시키는 촉매의 원리를 이해한다. B. Principles
www.happycampus.com
전기분해와 전기도금
일반화학실험2 전기분해와 전기도금 레포트 레포트
A. Objectives 전기 에너지를 이용해서 일어나는 화학 반응에 대하여 알아본다. 전기 분해, 전기 도금, 패러데이의 법칙에 대해 이해한다. B. Principles & Methods 전기분해란 전극을 통해서 전원에서 공
www.happycampus.com
의약품합성-아스피린
일반화학실험2 의약품합성-아스피린 레포트 레포트
A. Objectives 가장 성공적인 의약품의 하나인 아스피린을 합성하여 유기 합성의 의미를 배운다. B. Principles & Methods 유기합성이란 탄소 화합물을 중심으로 하는 유기 화합물의 인공적 합성이다. 탄
www.happycampus.com
시계반응
일반화학실험2 시계반응 레포트 레포트
A. Objectives 시계 반응을 이용해서 반응 속도의 차이가 큰 반응 단계가 연속적으로 일어나는 화학 반응의 특성을 알아본다. B. Principles & Methods 지금까지 개발된 시계 반응에는 여러 종류가 있는데,
www.happycampus.com
🧪 이외에도 많은 일반화학실험 글들은 Category [대학생활-대학공부] 참고
▼ Exp8. 이산화탄소의 승화열 레포트 보러가기 ▼
일반화학실험 #8 이산화탄소의 승화열(Sublimation Heat of CO2) 보고서(리포트), 내용총정리
▼ Exp5. 탄산염 분석 레포트 보러가기 ▼ 일반화학실험#5 탄산염 분석(Analysis of Carbonate Salt) 보고서(레포트), 내용총정리 ▼Exp4. 몰질량 측정 보러가기▼ 2021.07.26 - [입시 (학종, 생기부)/환경] - 일..
young-brightening.tistory.com
이 글의 저작권은 필자에게 있으며,
허가 없이 일부만을 발췌하더라도
법적인 제재를 받을 수 있음을 밝힙니다.
Copyright ⓒ 2022 All rights reserved by @young_claudialee.
All pictures and contents cannot be copied without permission.
'대학생활 > 대학공부' 카테고리의 다른 글
| [토양오염학 실습] 토양 채취 (0) | 2024.01.15 |
|---|---|
| Global Land Outlook Report(UNCCD 유엔 사막화 방지 협약) 보고서 요약정리 (2) | 2023.12.22 |
| 공학설계 특별수업(3D Modeling, 가새골조 의자만들기, 은박지 소품제작) (4) | 2022.07.31 |
| 일반화학실험 #8 이산화탄소의 승화열(Sublimation Heat of CO2) 보고서(리포트), 내용총정리 (8) | 2022.05.22 |
| 만점레포트:두교황 영화감상문 (기독교와세계) (27) | 2021.12.24 |
| [고급영어]만점받은 영어에세이 예시-아카데믹라이팅, contrast essay:The Differences between Plastics and Bioplastics (31) | 2021.12.16 |
| 일반화학실험 #4 몰질량 측정(Molar Mass Determination) 내용총정리 (19) | 2021.07.26 |
| 일반화학실험#2 재결정과 거르기(Recrystallization and filtration) 보고서(리포트), 내용총정리 (10) | 2021.05.25 |



